Síndrome Mielodisplásica de Baixo Risco
PROTOCOLO CÍNICO E DIRETRISE TERAPÊUTICA DE SÍNDROME MIELODISPLÁSICA DE BAIXO RISCO (Clique Aqui)
FLUXOGRAMA PARA SÍNDROME MIELODISPLÁSICA DE BAIXO RISCO (Clique Aqui)
FLUXO DE ACESSO AOS MEDICAMENTOS PARA SÍNDROME MIELODISPLÁSICA DE BAIXO RISCO (Clique Aqui)
CLASSIFICAÇÃO ESTATÍSTICA INTERNACIONAL DE DOENÇAS E PROBLEMAS RELACIONADOS À SAÚDE (CID-10)
D46.0 Anemia refratária sem sideroblastos
D46.1 Anemia refratária com sideroblastos
D46.4 Anemia refratária, não especificada
D46.7 Outras síndromes mielodisplásicas
Atenção: Para consultar as atualizações dos medicamentos e CID-10 desta patologia, acessar o SISTEMA
DE GERENCIAMENTO DA TABELA UNIFICADA DE PROCEDIMENTOS (SIGTAP): http://sigtap.datasus.gov.br
Medicamentos
- ALFAEPOETINA 10.000 UI INJETAVEL (POR FRASCO-AMPOLA) - Grupo 1A
- FILGRASTIM 300 MCG INJETAVEL (POR FRASCO AMPOLA OU SERINGA PREENCHIDA) - Grupo 1A
Documentos necessários
- Cópia do Cartão Nacional de Saúde (CNS) do paciente;
- Cópia de documento de identidade e CPF do paciente;
- Cópia do comprovante de residência; (em nome do paciente ou responsável legal pelo paciente)
- Laudo para Solicitação de Medicamentos do Componente Especializado (LME), adequadamente preenchido (renovar SEMESTRALMENTE);
- Prescrição médica devidamente preenchida, assinada e carimbada pelo médico. (As prescrições médicas devem obedecer as normas sanitárias vigentes para cada tipo de medicamento solicitado.(LEI Nº 13.732, DE 8 DE NOVEMBRO DE 2018;PORTARIA 344, de 1998;RESOLUÇÃO – RDC Nº 20, DE 5 DE MAIO DE 2011 e outros);
- Termo de Esclarecimento e Responsabilidade -TER;(Clique Aqui) assinado pelo médico e paciente.
- Formulário de Acesso ao medicamento para Síndrome Mielodisplásica de Baixo Risco, preenchido, assinado e carimbado pelo médico do paciente. (Clique Aqui)
- Relatório médico com CID-10, informando:
- 1. Diagnóstico clínico do paciente, de acordo com os critérios clínicos do PCDT da patologia: Para Alfaepoetina:( - Adultos (idade maior ou igual a 18 anos); E - Usuários com SMD de baixo risco e anemia sintomática (Hb menor ou igual a 10 g/L). Para Filgrastim:(- Adultos (idade maior ou igual a 18 anos); E - Usuários com síndrome mielodisplásica de baixo risco; E - Contagem de neutrófilos abaixo de 0,5 x 10 9 /L e infecções resistentes ou infecções de repetição; OU - Diagnóstico de anemia e que não apresentem resposta eritroide satisfatória após uso de alfaepoetina durante 16 semanas.
- 2. Ausência de critério de exclusão para uso do medicamento, conforme PCDT de Síndrome Mielodisplásica de Baixo Risco.
Exames para abertura de processo
- Relato no Formulário Médico Obrigatório da classificação de risco da SMD (pontuação do IPSS -
International Prognostic Score System e pontuação do WPSS - WHO classification-based prognostic scoring
system);
- Hemograma completo, incluindo contagem de plaquetas e reticulócitos; (validade 3 meses)
- Mielograma; Coloração para ferro na medula óssea (pesquisa de sideroblastos em anel); (validade 12 meses)
- Citogenética convencional da medula óssea com bandeamento G ou hibridização in situ por fluorescência (FISH); (validade 12 meses)
- Histopatológico da medula óssea (com pesquisa de fibrose medular - coloração pela reticulina) (validade 12 meses)
Exames de monitoramento
Para Alfaepoetina:
Hemograma a cada quinze dias, durante o primeiro mês, seguido de hemograma mensal até a 24ª
semana de tratamento.
Para Filgrastim:
Hemogramas semanais ou quinzenais até a definição da dose ideal de acordo com a necessidade
e resposta. Para correção de neutropenia, a dose de filgrastim deve ser ajustada para manter
contagem de neutrófilos acima de 1 x 10⁹/L
Para uso associado à Alfaepoetina, a dose de Filgrastim deve ser adequada para dobrar a contagem inicial
de leucócitos nos usuários com contagem de leucócitos abaixo de 1,5 x 10⁹ /L no início do tratamento, ou
para manter a contagem de leucócitos nos usuários com leucócitos entre 6 e 10 x 10⁹ /L no início do
tratamento. Caso o usuário tenha atingido a resposta eritróide completa ou parcial, seu uso deve ser mantido em terapia
de longo prazo na dose mínima necessária para manter a resposta ou até que a resposta seja perdida.
Deve se interromper o uso de Filgrastim na ausência de resposta eritróide após oito semanas de seu
uso associado à Alfaepoetina
Unidades de Referência
- Capital e Região Metropolitana
- Centro Estadual de Referência às Pessoas com Doença Falciforme- RILZA VALENTIM
- Endereco, Avenida Centenario no 801, Garcia, Salvador Bahia.
- Contatos Telefonicos:(71) 3339-6000/ (71) 3339-6027/ (71 )3339-6028
- Horário de atendimento:
- segunda a sexta-feira, das 07:00 horas as 17;00 horas (exceto feriados)
- E-mail: fatima.souto@hemoba.ba.gov.br
- Interior
- Bases Regionais de Saúde e Núcleos Regionais de Saúde (antigas DIRES)
Fluxo de acesso para Salvador
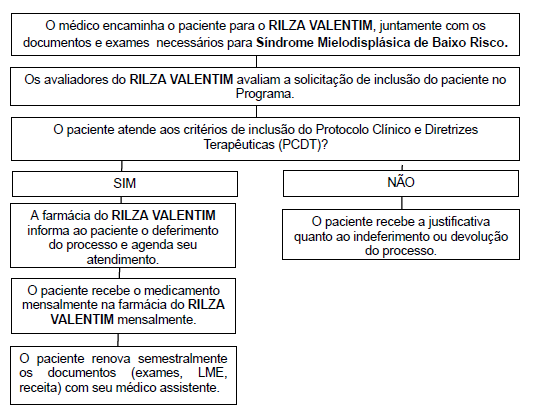
Fluxo de acesso para Núcleos Regionais de Saúde (NRS) e/ou Bases Regionais de Saúde (BRS) - Antigas Dires

Observações
- Especialidade Médica: Hematologia
- Para o uso de Filgrastim, serão excluídos usuários com contagem de neutrófilos acima de 10x10 9/L.
- CASOS ESPECIAIS:
Durante a gestação e durante o período de amamentação, as mulheres devem ser preferencialmente elegíveis para tratamento de suporte e necessitam ser avaliadas individualmente. A indicação de tratamento
medicamentoso deverá ser avaliada individualmente conforme riscos e benefícios específicos de cada medicamento.
Data da Atualização: 19/01/2026

