Protocolo Clínico e Diretrizes Terapêuticas da Atrofia Muscular Espinhal 5q Tipo 1 e 2 (Clique Aqui)
PCDT Resumido de Atrofia Muscular Espinhal 5q Tipo 1 e 2 (Clique aqui)
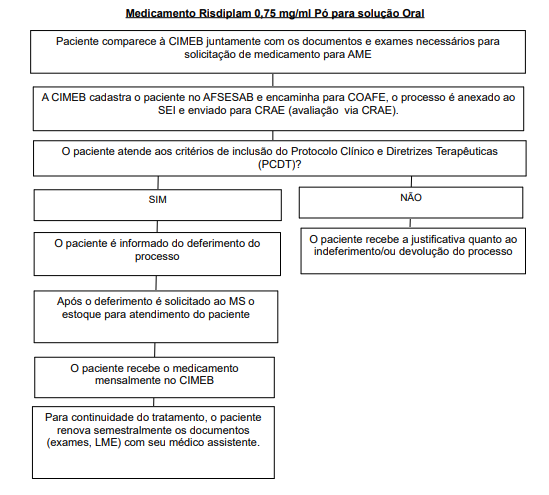
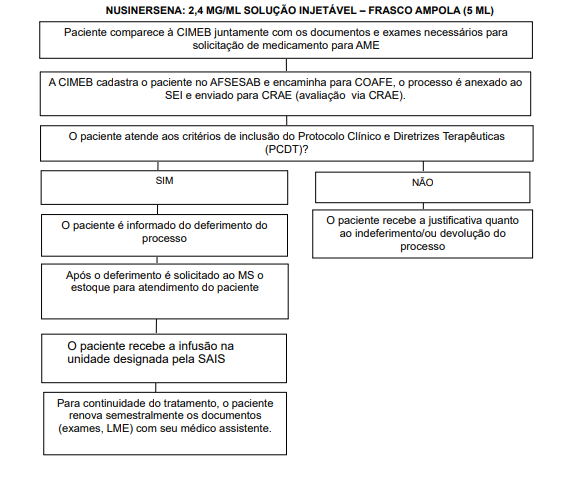
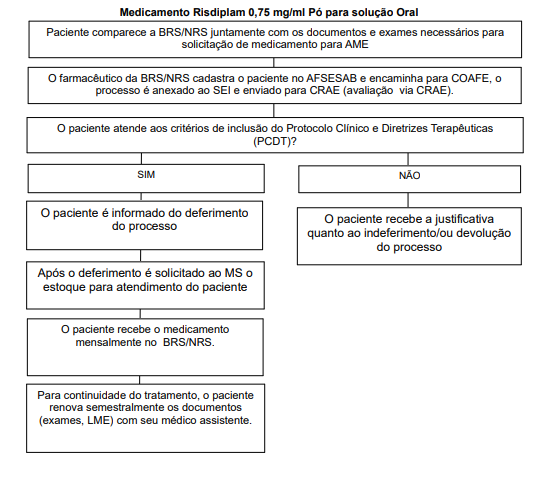
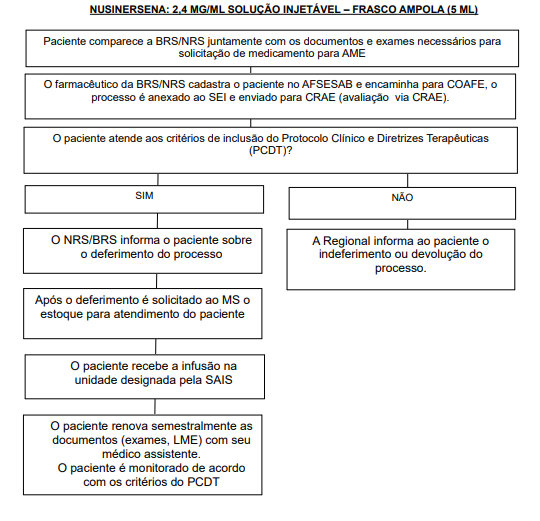
Fluxo de Acesso aos Medicamentos para Atrofia Muscular Espinhal 5q Tipo 1 e 2 (Clique Aqui)
CLASSIFICAÇÃO ESTATÍSTICA INTERNACIONAL DE DOENÇAS E PROBLEMAS RELACIONADOS À SAÚDE (CID-10)
G12.0 – Atrofia muscular espinal infantil tipo I (Werdnig-Hoffman)
G12.1 – Outras atrofias musculares espinais hereditárias
Atenção: Para consultar as atualizações dos medicamentos e CID-10 desta patologia, acessar o SISTEMA DE GERENCIAMENTO DA TABELA UNIFICADA DE PROCEDIMENTOS