Protocolo Clínico e Diretrizes Terapêuticas da Fibrose Cística – Manifestações Pulmonares (Clique Aqui).
PCDT Resumido de Fibrose Cística – Manifestações Pulmonares (Clique aqui)
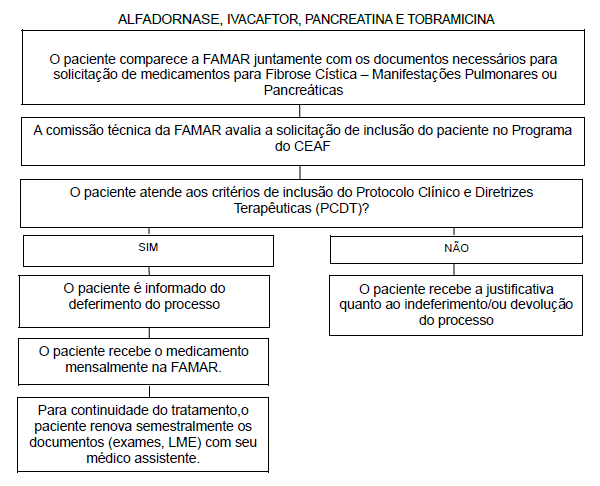
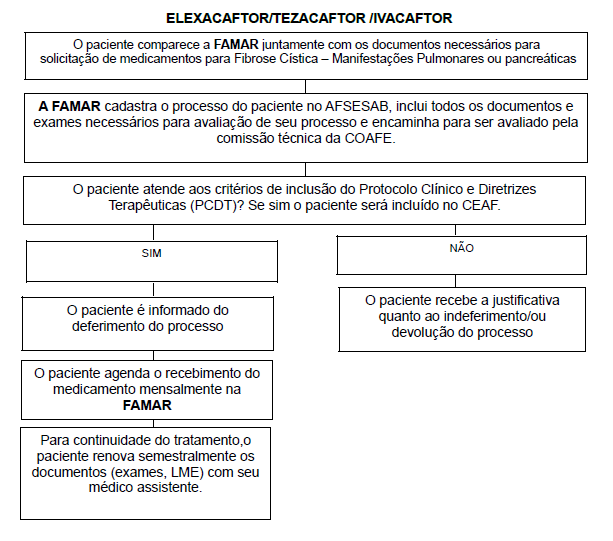
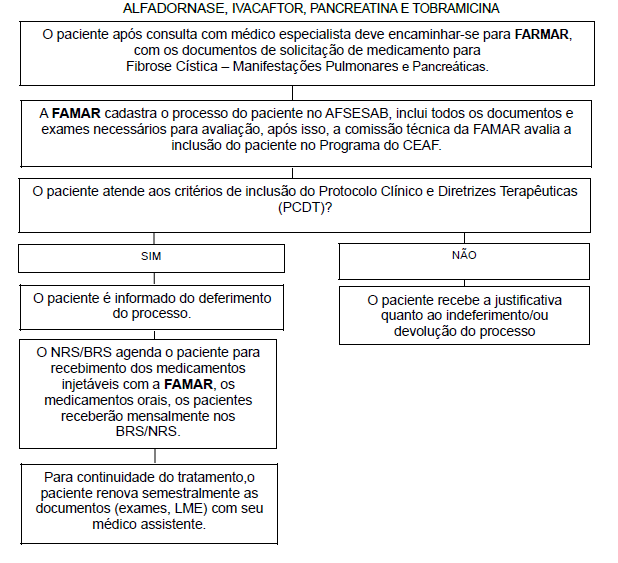
Fluxo de Acesso aos Medicamentos para Fibrose Cística – Manifestações Pulmonares (Clique Aqui)
CLASSIFICAÇÃO ESTATÍSTICA INTERNACIONAL DE DOENÇAS E PROBLEMAS RELACIONADOS À SAÚDE (CID-10)
E84.0 Fibrose cística com manifestações pulmonares
E84.1 Fibrose cística com manifestações intestinais
E84.8 Fibrose cística com outras manifestações
Atenção: Para consultar as atualizações dos medicamentos e de CID-10 desta patologia, favor acessar o SISTEMA DE GERENCIAMENTO DA TABELA UNIFICADA DE PROCEDIMENTOS (SIGTAP)