Medicamentos
- ALFAELOSULFASE 1 MG/ML SOLUÇÃO INJETÁVEL (POR FRASCO AMPOLA DE 5 ML) - Grupo 1A
Documentos necessários
- Cópia do Cartão Nacional de Saúde (CNS) do paciente;
- Cópia de documento de identidade e CPF do paciente;
- Cópia do comprovante de residência; (em nome do paciente ou responsável pelo paciente)
- Laudo para Solicitação de Medicamentos do Componente Especializado (LME), adequadamente preenchido (deve ser renovado SEMESTRALMENTE);
- Prescrição médica devidamente preenchida, assinada e carimbada pelo médico. (As prescrições médicas devem obedecer as normas sanitárias vigentes para cada tipo de medicamento solicitado.(LEI Nº 13.732, DE 8 DE NOVEMBRO DE 2018;PORTARIA 344, de 1998;RESOLUÇÃO – RDC Nº 20, DE 5 DE MAIO DE 2011 e outros);
- Termo de Esclarecimento e Responsabilidade -TER; assinado pelo médico e paciente.
- Relatório médico com CID-10, informando os critérios de inclusão de acordo com o PCDT:
- 1. Todos os pacientes que apresentarem pelo menos um dos sintomas ou sinais descritos no PCDT de MPS IV A.
- 2. Paciente com Suspeita Diagnóstica e tiverem o diagnóstico de MPS IV A confirmado de acordo com um dos critérios abaixo relacionados:
- - atividade da GALNS < 10% do limite inferior dos valores de referência em fibroblastos ou leucócitos E atividade de uma outra sulfatase (arilsulfatase A, arilsulfatase B, heparan N-sulfatase ou iduronatosulfatase) avaliada na mesma amostra e pelo mesmo método, apresentando valores normais; OU
- - atividade da GALNS < 10% do limite inferior dos valores de referência em papel-filtro, fibroblastos ou leucócitos E presença de mutações patogênicas em homozigose ou heterozigose composta no gene GALNS.
Exames para abertura de processo
- EXAMES OBRIGATÓRIOS:
- Atividade da GALNS e (validade indeterminada)
- Atividade, pelo menos uma, outra sulfatase, (arilsulfatase A, arilsulfatase B, heparan N-sulfatase ou iduronato-sulfatase) avaliada na mesma amostra e pelo mesmo método.(validade indeterminada)
- EXAMES COMPLEMENTARES: *Observações
- Pacientes que receberão o primeiro atendimento via CEAF devem disponibilizar todos os relatórios médicos de avaliação inicial.
- Abaixo estão descritas avaliações necessárias de acordo com apêndice B da Portaria Conjunta SCTIE/SAES/MS Nº 19, de 05 dezembro de 2019.
- AVALIAÇÃO NEUROLÓGICA:
- Exame neurológico (validade indeterminada)
- RNM do crânio (validade indeterminada)
- RNM da coluna (validade indeterminada)
- Velocidade de condução do nervo mediano
- Avaliação do neurodesenvolvimento
- AVALIAÇÃO OFTALMOLÓGICA :
- Acuidade visual,
- Exame de Retina
- Exame da Córnea
- AUDIOMETRIA
- AVALIAÇÃO FUNCIONAL
- Ecocardiograma (validade indeterminada)
- Eletrocardiograma (validade indeterminada)
- TC12M (validade indeterminada)
- CVF/VEF1 (Espirometria) (validade indeterminada)
- Polissonografia (validade indeterminada)
- AVALIAÇÃO DA MOBILIDADE ARTICULAR
- RAIO-X ÓSSEO ( Laudo) (validade indeterminada)
Exames de monitoramento
- Atividade enzimática ( Para pacientes que fizeram transplante de células-tronco hematopoéticas)
- TC6M ( teste da caminhada de 6 minutos )
- Espirometria (CVF/VEF1),
- Níveis urinários de GAGs,
- Ecocardiograma;
- Relatório Médico com CID-10 incluindo; 1. História médica(descrição clínica detalhada dos sinais e sintomas, informando se o paciente apresenta regressão neurológica, conforme PCDT de Mucopolissacaridose Tipo IV;
- 2. Aconselhamento Genético ;
- 3. Determinação da adesão ao acompanhamento/tratamento;
- 4. Peso/altura;
- 5. Pressão arterial
- 6. Informações sobre a Hepatimetria (exame físico);
- 7. Questionário de qualidade de vida validado;
- 8. Informações de adesão ao tratamento, e número de infusões durante o período.
- Periodicidade: a cada seis meses.
Unidades de Referência
CAPITAL:
CIMEB - Centro de Infusões e Medicamentos Especializados da Bahia
Parque Solar Boa Vista
End: Av. Laurindo Régis, s/nº -Engenho Velho de Brotas, Salvador - BA, CEP 40250-240
Tel da Farmácia: 3116-4935/31171645
Horário: 7h às 18h
E-mail:cimeb@saude.ba.gov.br
INTERIOR:
Bases Regionais de Saúde e Núcleos Regionais de Saúde (antigas DIRES)
UNIDADE DE INFUSÃO
A unidade de infusão será definida após a avaliação inicial dos documentos e exames do paciente.
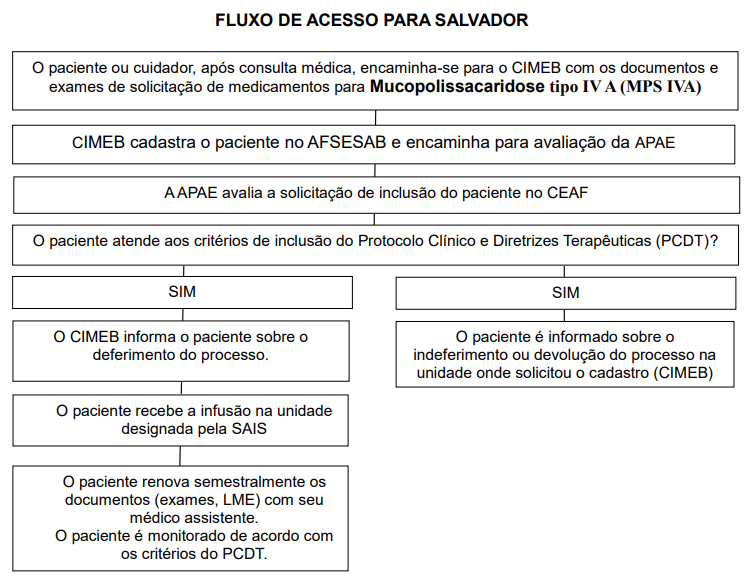
Fluxo de acesso para Salvador
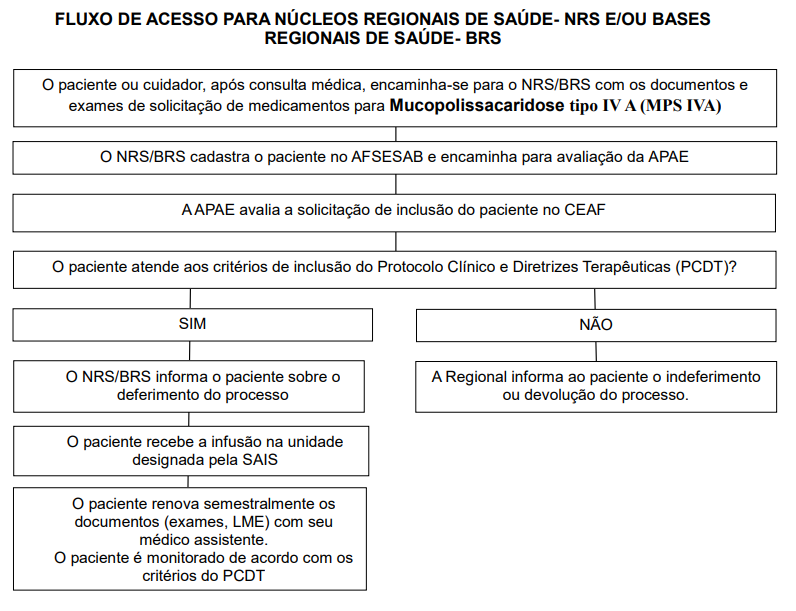
Fluxo de acesso para Núcleos Regionais de Saúde (NRS) e/ou Bases Regionais de Saúde (BRS) - Antigas Dires