Amiloidoses Associadas à Transtirretina
Protolo Clínico e Diretrizes Terapêuticas de Amiloidoses Associadas à Transtirretina (clique aqui)
Fluxo de Acesso aos Medicamentos para Amiloidoses Associadas à Transtirretina (Clique Aqui)
CLASSIFICAÇÃO ESTATÍSTICA INTERNACIONAL DE DOENÇAS E PROBLEMAS RELACIONADOS À SAÚDE (CID-10)
- E85.0 Amiloidose heredofamiliar não-neuropática.
- E85.1 Amiloidose heredofamiliar neuropática.
- E85.8 Outras Amiloidoses.
Atenção: Para consultar as atualizações dos medicamentos e CID-10 desta patologia, acessar o SISTEMA DE GERENCIAMENTO DA TABELA UNIFICADA DE PROCEDIMENTOS (SIGTAP)
Medicamentos
- TAFAMIDIS 20 MG CÁPSULA - Grupo 1A
- TAFAMIDIS 61 MG (POR CÁPSULA), Grupo 1A
Documentos necessários
- Cópia do Cartão Nacional de Saúde (CNS) do paciente;
- Cópia de documento de identidade e CPF do paciente;
- Cópia do comprovante de residência; (em nome do paciente ou responsável pelo paciente)
- Laudo para Solicitação de Medicamentos do Componente Especializado LME (Clique Aqui), adequadamente preenchido (renovar SEMESTRALMENTE);
- Prescrição médica devidamente preenchida, assinada e carimbada pelo médico. (As prescrições médicas devem obedecer as normas sanitárias vigentes para cada tipo de medicamento solicitado.(LEI Nº 13.732, DE 8 DE NOVEMBRO DE 2018;PORTARIA 344, de 1998;RESOLUÇÃO – RDC Nº 20, DE 5 DE MAIO DE 2011 e outros)
- Termo de Esclarecimento e Responsabilidade -TER; (Clique Aqui) preenchido adequadamente, assinado e carimbado pelo médico e assinado pelo paciente.
- Formulário de Acesso ao Medicamento para Amiloidoses Associadas à Transtirretina, (Clique Aqui), preenchido, assinado e carimbado pelo médico OU
- Relatório médico com CID-10, informando: 1. Sinais e sintomas apresentados pelo paciente, 2. Ausência de critério de exclusão para uso do medicamento, conforme PCDT de Amiloidoses Associadas à Transtirretina
Exames para abertura de processo
Para uso de Tafamidis meglimina 20 mg (CID-10 E85.1): Os pacientes devem apresentar polineuropatia amiloidótica hereditária (familiar) sintomática em estágio inicial (estágio I de coutinho ) e não terem sido submetidos à transplante hepático (anexar o exame que comprove a situação clínica do paciente))
- Teste genético comprovando a mutação em TTR;
- B-HCG (para indivíduos com potencial gestacional, excetuando-se aqueles com histórico de histerectomia ou esterilidade comprovada) (validade do exame 01 mês).
Para uso de Tafamidis 61 mg (CID-10 E85.0 ou E85.8): Os pacientes devem apresetnar cardiomiopatia associada à TTR (selvagem ou hereditária), classe NYHA II ou III e idade acima de 60 anos (anexar o exame que comprove a situação clínica do paciente).
- B-HCG (para indivíduos com potencial gestacional, excetuando-se aqueles com histórico de histerectomia ou esterilidade comprovada) (validade do exame 01 mês);
- Teste genético comprovando a mutação em TTR, somente pacientes com mutação genética (hereditária).
- Exame que comprove cardiomiopatia associado à TTR:
- Eletrocardiograma (validada indeterminada) OU;
- Ecocardiografia transtorácica, (validade indeterminada) OU;
- Ressonância magnética de coração, cintilografia cardíaca com pirofosfato (ou outro marcador específico para a TTR) e monitoramento pelo sistema Holter OU;
- BNP ou NY-próBNP (porção N-terminal do precursor de BNP) ou dosagem de troponina.
Exames de monitoramento
- Ureia, Creatinina, Ácido úrico, Taxa de Filtração glomerular, Proteinúria em 24 horas Periodicidade: a cada 6 meses.
Unidades de Referência
Capital e Região Metropolitana:
CIMEB – Centro de Infusões e Medicamentos Especializados da Bahia
Parque Solar Boa vista
End: Av. Laurindo Régis, s/nº - Engenho Velho de Brotas, Salvador - BA, CEP 40.240-550
Tel: da Farmácia: 3116-4935/31171645
Horário: 8h às 18h
E-mail:cimeb@saude.ba.gov.br
Interior
Bases Regionais de Saúde e Núcleos Regionais de Saúde (antigas DIRES)
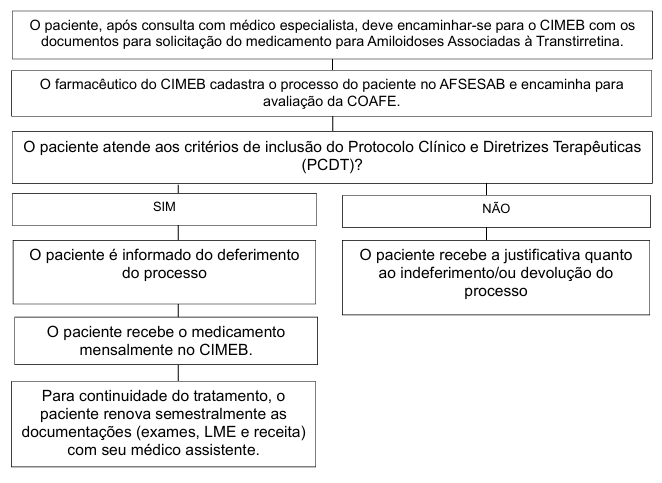
Fluxo de acesso para Salvador
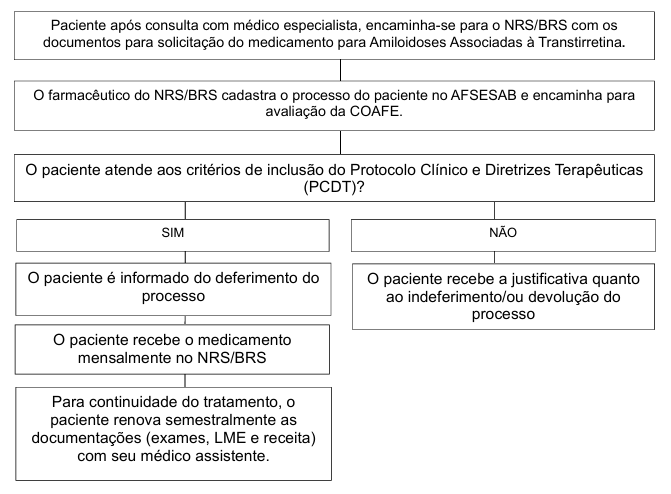
Fluxo de acesso para Núcleos Regionais de Saúde (NRS) e/ou Bases Regionais de Saúde (BRS) - Antigas Dires
Observações
- O diagnóstico da PAF-TTR deve ser determinado, a partir do quadro clínico do paciente, por especialistas na área de neurologia ou cardiologia.
- Em relação ao uso de Tafamidis, serão excluídos gestantes e lactantes.
- O uso concomitante de Tafamidis 20 mg e Tafamidis 61 mg não é preconizado por este Protocolo. Assim, pacientes em uso de Tafamidis meglumina 20 mg estão excluídos do uso de Tafamidis 61 mg. Do mesmo modo, pacientes em uso de Tafamidis 61 mg estão excluídos do uso de Tafamidis meglumina 20 mg.
- Os pacientes com amilodoise familiar (hereditária) associada à transtirretina com comprometimento misto (neurológico e cardíaco) que já estejam em uso de Tafamidis meglumina 20 mg podem migrar para o uso de Tafamidis 61 mg, caso seja a escolha terapêutica da equipe médica assistente e respeitando os demais critérios de inclusão.
- Idade: A partir de 18 anos.
- Data da Atualização: 11/03/2026

