Síndrome de Falência Medular
Protocolo Clínico e Diretrizes Terapêuticas de Síndrome de Falência Medular (clique aqui)
PCDT de Síndrome de Falência Medular Resumido (clique aqui)
Fluxo de Acesso aos Medicamentos para Falência medular (Clique aqui)
CLASSIFICAÇÃO ESTATÍSTICA INTERNACIONAL DE DOENÇAS E PROBLEMAS RELACIONADOS À SAÚDE (CID-10)
D60.0 Aplasia pura de glóbulos vermelhos adquirida crônica
D60.1 Aplasia pura de glóbulos vermelhos adquirida transitória
D60.8 Outras anemias aplásticas especificadas e outras síndromes de falha da medula óssea
D61.0 Anemia Aplástica Constitucional
D61.1 Anemia aplástica induzida por drogas
D61.2 Anemia aplástica devida a outros agentes externos
D61.3 Anemia aplástica idiopática
D61.8 Outras anemias aplásticas especificadas
D70 Agranulocitose
Z94.8 Outros órgãos e tecidos transplantados
Atenção: Para consultar as atualizações dos medicamentos e de CID-10 desta patologia, favor acessar o SISTEMA DE GERENCIAMENTO DA TABELA UNIFICADA DE PROCEDIMENTOS (SIGTAP)
Medicamentos
- CICLOFOSFAMIDA 50 MG (POR DRAGEA) - Grupo 2
- CICLOSPORINA 100 MG (POR CAPSULA) - Grupo 2
- CICLOSPORINA 100 MG/ML SOLUCAO ORAL (POR FRASCO DE 50 ML) - Grupo 2
- CICLOSPORINA 25 MG (POR CAPSULA) - Grupo 2
- CICLOSPORINA 50 MG (POR CAPSULA) - Grupo 2
- ELTROMBOPAGUE OLAMINA 25 MG (POR COMPRIMIDO) - Grupo 1B
- ELTROMBOPAGUE OLAMINA 50 MG (POR COMPRIMIDO) - Grupo 1B
- FILGRASTIM 300 MCG INJETAVEL (POR FRASCO AMPOLA OU SERINGA PREENCHIDA) - Grupo 1A
- IMUNOGLOBULINA HUMANA 5,0 G INJETAVEL (POR FRASCO) - Grupo 1A
Documentos necessários
- Cópia do Cartão Nacional de Saúde (CNS) do paciente;
- Cópia de documento de identidade e CPF do paciente;
- Cópia do comprovante de residência; (em nome do paciente ou responsável pelo paciente), se o comprovante estiver em nome de Terceiros (Clique Aqui)
- Laudo para Solicitação de Medicamentos do Componente Especializado LME (Clique Aqui), adequadamente preenchido (renovar SEMESTRALMENTE);
- Prescrição médica devidamente preenchida, assinada e carimbada pelo médico. (As prescrições médicas devem obedecer as normas sanitárias vigentes para cada tipo de medicamento solicitado.(LEI Nº 13.732, DE 8 DE NOVEMBRO DE 2018;PORTARIA 344, de 1998;RESOLUÇÃO – RDC Nº 20, DE 5 DE MAIO DE 2011 e outros).
- Termo de Esclarecimento e Responsabilidade -TER;(Clique Aqui) preenchido e assinado pelo médico e assinado pelo paciente.
- Relatório médico com CID-10, informando os seguintes dados:1. História clínica do paciente de acordo com os critérios de inclusão do PCDT de Síndrome de Falência Medular, para cada medicamento. 2. Ausência de todos os critérios de exclusão para uso do medicamento prescrito, conforme PCDT de Síndrome de Falência Medular
Exames para abertura de processo
- Para pacientes com Aplasia Pura de Série Vermelha:
- Para Ciclofosfamida CIDs - (D60.0, D60.1, D60.8)
- Hemograma, plaquetas, (validade 3 meses)
- Contagem de Reticulócitos, (validade 3 meses)
- Imunofenotipagem para doenças linfoproliferativas; (validade 12 meses)
- Sorologias para HIV, (validade 12 meses)
- Sorologia para Hepatite B, (validade 12 meses)
- Sorologia para Hepatite C, EBV e CMV; (validade 12 meses)
- FAN (fator antinuclear), (validade 12 meses)
- Fator Reumatoide; (validade indeterminada)
- Biópsia de medula óssea, (validade indeterminada)
- Mielograma e análise Citogenética; (validade 12 meses)
- Tomografia computadorizada de tórax para exclusão de timoma;(validade 12 meses)
- Beta-HCG (pacientes < 55 anos). (validade 1 mês)
- Para pacientes com Anemia aplástica:
- Para Ciclosporina CIDs - (D60.0, D60.1, D60.8, D61.0, D61.1, D61.2, D61.3, D61.8, Z94.8)
- Hemograma, com contagem de plaquetas e (validade 3 meses)
- Contagem de Reticulócitos; (validade 3 meses)
- Sorologias para HIV, (validade 12 meses)
- Sorologia para hepatite B, (validade 12 meses)
- Sorologia para hepatite C, EBV e CMV; (validade 12 meses)
- PPD; (validade 3 meses)
- FAN (fator antinuclear), (validade 12 meses)
- Fator Reumatóide; (validade indeterminada)
- Dosagem de vitamina B12 e (validade 3 meses)
- Dosagem de Ácido Fólico; (validade 3 meses)
- Análise morfológica da medula óssea sem sinais de síndrome mielodisplásica hipoplástica;
- A pesquisa de células GPI (glicofosfatidilinusitol) negativa para o diagnóstico de hemoglobinúria paroxística noturna deve ser realizada em todos os pacientes com suspeita de Anemia Aplástica adquirida;
- Beta-HCG (pacientes < 55 anos).(validade 1 mês)
- Para Imunoglobulina: CIDs - D60.0, D60.1, D60.8
- Hemograma com Hb menor que 7 g/dL;(validade 3 meses)
- Creatinina; (validade 3 meses)
- Biópsia de MO com proeritroblastos vacuolados gigantes; OU (validade indeterminada)
- Anticorpos Anti-B19 IgM ou detecção de DNA-viral por biologia molecular; OU
- (validade 12 meses)
- Eletroforese de proteínas do sangue (para pacientes com hipoglobulinemia).
- (validade 12 meses)
- Para ELTROMBOPAGUE: CIDs - D61.0, D61.1, D61.2, D61.3, D61.8.
- Hemograma, com contagem de plaquetas e reticulócitos; (validade 3 meses)
- Sorologias para HIV, (validade 12 meses)
- Sorologia para hepatite B, (validade 12 meses)
- Sorologia para hepatite C, (validade 12 meses)
- Sorologia para EBV e (validade 12 meses)
- Sorologia para CMV; (validade 12 meses)
- Reação de Mantoux -PPD; (validade 12 meses)
- FAN (fator antinuclear), (validade 12 meses)
- Fator Reumatoide; (validade indeterminada)
- Dosagem de vitamina B12 e (validade 3 meses)
- Ácido fólico; (validade 3 meses)
- AST/TGO (validade 3 meses)
- ALT/TGP e (validade 3 meses)
- Bilirrubinas; (validade 3 meses)
- - Análise morfológica da medula óssea sem sinais de síndrome mielodisplásica hipoplástica;
- - Pesquisa de células GPI (glicofosfatidilinusitol) negativa para o diagnóstico de hemoglobinúria paroxística noturna.
- Para FILGRASTIM: CIDs - D70, D610, D61.1, D612, D613 e D618
- *A dispensação do medicamento Filgrastim para as CID-10 D61.0, D61.1, D61.2, D61.3, D61.8 será permitida apenas como terapia adjuvante ao tratamento antimicrobiano para pacientes com infecções graves.
- Relato médico descrevendo a condição clínica, com comorbidades, doença de base, intenção de tratamento (curativo ou paliativo);
- Hemograma com contagem de neutrófilos e plaquetas.(validade 3 meses)
- Contagem de reticulócitos; (validade 3 meses)
- Biópsia de medula óssea com aumento de promielócitos e mielócitos e diminuição de metamielócitos, bastões e neutrófilos. (validade indeterminada)
Exames de monitoramento
- Para Ciclofosfamida:
- Preconiza-se avaliação mínima com hemograma e contagem de reticulócitos a cada retorno de avaliação, em intervalos de 5 a 7 dias no início do tratamento, e a cada 2 dias se a contagem cair abaixo de 3000 células/microlitro (células/mm 3 ).
- Para tratamento a longo prazo, monitoramento em intervalos de cerca de 14 dias geralmente é suficiente.
- Outros exames laboratoriais devem ser solicitados conforme a doença de base e a terapia imunossupressora em uso.
- Deve ser usado com precaução em pacientes idosos e em pacientes que tenham sido previamente submetidos a radioterapia. Os pacientes com imunidade baixa, diabetes mellitus, doenças hepáticas ou doenças renais crônicas e doenças cardíacas pré-existentes também devem ser monitorados de perto.
- Não deve ser administrado em pacientes com contagem de neutrófilos menor ou igual a 1500 células/mm3 e/ou contagem de plaquetas abaixo de 50.000 células/mm3 .
- Para Ciclosporina:
- Preconiza-se Hemograma e contagem de reticulócitos a cada retorno de avaliação.
- A cada 6 meses devem ser realizados hemograma, contagem de reticulócitos, análise de mielograma, biópsia de medula óssea e análise de cariótipo.
- Os pacientes em uso de Ciclosporina devem ter o nível sérico de creatinina, ureia, sódio, potássio e magnésio monitorados durante as reavaliações do nível sérico de Ciclosporina, visto que o medicamento é nefrotóxico e seu uso está associado à espoliação de magnésio.
- O nível sérico de Ciclosporina deve ser monitorado semanalmente até a obtenção de nível sérico adequado e, posteriormente, a cada duas a quatro semanas para as consultas com o médico assistente.
- Para os pacientes que apresentam resposta clínica, a Ciclosporina deve ser desmamada lentamente em 18 meses, totalizando 24 meses de tratamento.
- O monitoramento cuidadoso da pressão arterial, dos parâmetros adequados para avaliar a função hepática é necessário. -Outros exames laboratoriais devem ser solicitados conforme a doença de base e a terapia imunossupressora em uso.
- Para ELTROMBOPAGUE:
- Os pacientes submetidos à imunossupressão com GAT, Ciclosporina e Eltrombopague devem ser reavaliados após 6 meses, a fim de verificar sua resposta ao tratamento, por meio de hemograma, contagem de reticulócitos, análise de mielograma, biópsia de medula óssea e análise de cariótipo.
- O Eltrombopague pode alterar a função hepática, dessa forma é necessário a monitorização de lesão e função hepática, com dosagem de AST/TGO, ALT/TGP, Gama Glutamil Transferase (Gama-GT), Fosfatase Alcalina e Bilirrubinas.
- Para FILGRASTIM:
- Hemograma completo e plaquetas semanalmente até que a contagem de neutrófilos esteja acima de 1.000/μL. Uma vez atingido este nível, a dose de Filgrastim deve ser titulada para que o paciente utilize a menor dose terapêutica capaz de manter a contagem de neutrófilos acima de 1000/μL. Quando a contagem de neutrófilos dos pacientes estiver estabilizada, deve-se realizar hemograma a cada 1 a 3 meses para reavaliação.
- O uso do medicamento também deve considerar a avaliação de risco global do paciente, incluindo contagem de neutrófilos (atual ou prevista); condições relacionadas ao paciente (fatores de risco): idade, presença de comorbidades; condições clínicas significativas, história de radioterapia ou quimioterapia prévias; doença de base; toxicidade do tratamento; e intenção do tratamento (curativo ou paliativo).
- Não deve ser administrado 24 horas (1 dia) antes ou após a quimioterapia ou radioterapia.
- Diversas alterações genéticas, tanto de caráter autossômico como recessivo, estão relacionadas à neutropenia congênita grave, com riscos diferentes de evolução clonal para síndrome mielodisplásica e leucemia mieloide aguda.
- Alguns grupos internacionais preconizam avaliação do mielograma e cariótipo anualmente.
- Caso pacientes em uso de Filgrastim apresentem efeitos adversos, os médicos devem avaliar o risco-benefício do tratamento e, se necessário, interrompê-lo.
- Suspender o uso em casos de leucocitose (leucócitos acima 10.000/mm3 ).
Unidades de Referência
- Capital e Região Metropolitana
- Centro Estadual de Referência às Pessoas com Doença Falciforme- RILZA VALENTIM
- Endereco, Avenida Centenario no 801, Garcia, Salvador Bahia.
- Contatos Telefonicos:(71) 3339-6000/ (71) 3339-6027/ (71 )3339-6028
- Horário de atendimento:
- segunda a sexta-feira, das 07:00 horas as 17;00 horas (exceto feriados)
- E-mail: fatima.souto@hemoba.ba.gov.br
- Hospital Universitário Professor Edgard Santos - HUPES (apenas para os pacientes cadastrados no HUPES)
- R. Dr. Augusto Viana, s/n - Canela, Salvador - BA, 40110-060
- Telefone:(71) 3646-3400
- Horário: 07:00 às 19:00 horas
- Interior
- Bases Regionais De Saúde E Núcleos Regionais De Saúde (antigas DIRES)
Fluxo de acesso para Salvador

Fluxo de acesso para Núcleos Regionais de Saúde (NRS) e/ou Bases Regionais de Saúde (BRS) - Antigas Dires
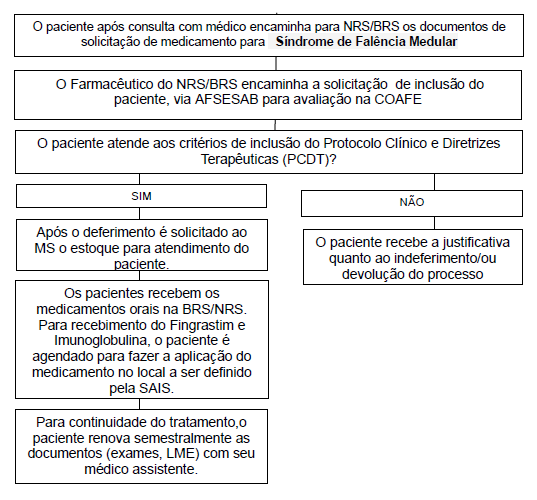
Observações
Devem ser observados os critérios de inclusão e exclusão de pacientes neste Protocolo, a duração e a monitorização do tratamento, bem como a verificação periódica das doses de medicamento(s) prescrito(s) e dispensado(s), a adequação de uso desse(s) medicamentos(s) e o acompanhamento pós-tratamento.
A cada avaliação clínica, atentar para possíveis sinais clínicos, como esplenomegalia, urticária, hipotireoidismo e alterações oculares.
Data atualização: 19/01/2026

